>>COVID-19 : le Japon va lancer une nouvelle campagne de dépistage d'anticorps
>>Les États-Unis espèrent commencer à vacciner à la mi-décembre
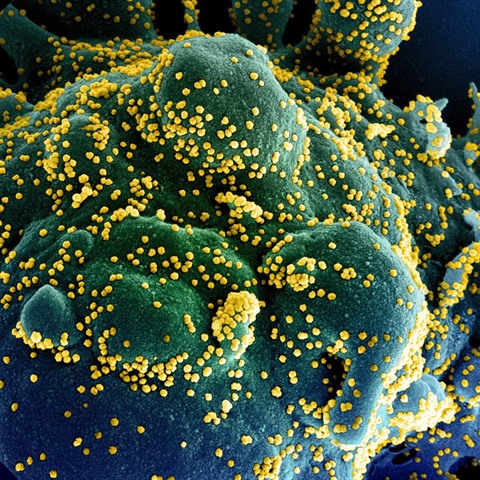 |
| Une cellule humaine infectée par le SARS-CoV-2. |
| Photo : AFP/VNA/CVN |
Les résultats ont été qualifiés de "très encourageants" par Stephen Evans, un professeur de pharmacoépidémiologie à la London School of Hygiene and Tropical Medicine.
"Il s'agit des premiers médicaments antiviraux qui marchent de manière prouvée lors de la première phase de la maladie, juste après que le virus a infecté une personne mais avant qu'il ait eu le temps de provoquer des dégâts", a-t-il ajouté.
L'entreprise de biotechnologie Regeneron a de son côté annoncé des résultats intérimaires positifs pour son essai de phase 3 sur le REGEN-COV, une combinaison de deux anticorps, pour une utilisation préventive, c'est-à-dire avant même qu'il y ait infection par le virus.
Grand potentiel
Concernant le traitement d'Eli Lilly, les résultats signifient que l'essai de phase 3 auquel ont participé 1.035 personnes a atteint son principal objectif; l'étude a aussi atteint ses objectifs secondaires de réduire la charge virale des patients et leur temps de convalescence.
Les patients ont reçu soit un placebo, soit la combinaison bamlanivimab-etesevimab, les deux anticorps, à 2,8 grammes chacun.
Onze hospitalisations ont été enregistrées chez les patients ayant reçu le traitement, soit 2,1% de ce groupe.
Chez les personnes ayant reçu un placebo, il y a eu 36 décès ou hospitalisations, soit 7% de ce groupe.
Le traitement représente donc une réduction de risque de 70%. Le résultat est suffisamment important en termes statistiques pour signifier qu'il est peu probable qu'il soit dû au hasard.
Dix décès ont en tout été enregistrés, tous au sein du groupe ayant pris un placebo. Aucun ne s'est produit chez les personnes ayant pris le traitement.
"Le bamlanivimab et l'etesevimab, ensemble, ont le potentiel pour être un traitement important réduisant de manière significative les hospitalisations et la mort chez les patients Covid à haut risque", a déclaré le principal responsable scientifique du groupe, Daniel Skovronsky.
Le groupe pharmaceutique a indiqué qu'il allait continuer à étudier le traitement dans le cadre d'un autre essai pour voir si une dose inférieure produit le même effet.
Un article d'évaluation par les pairs est encore attendu.
 |
| Une chaîne de production du vaccin contre le COVID-19, Sputnik V, dans une compagnie de produits pharmaceutiques à Karaganda (Kazakhstan), le 24 décembre 2020. |
| Photo : Xinhua/VNA/CVN |
Difficultés logistiques
Ces anticorps sont une version, fabriquée en laboratoire, des défenses immunitaires du corps humain.
Chez Regeneron, les données analysées portent sur environ 400 patients, dont la moitié a reçu 1,2 grammes du traitement par injection sous-cutanée, l'autre un placebo.
Sur les 223 patients ayant reçu le placebo, huit ont plus tard été infectés par le COVID-19 tout en présentant des symptômes, ce qui n'a été le cas d'aucune des 186 personnes ayant reçu le REGEN-COV, soit une réduction de 100% des infections symptomatiques.
Le traitement a aussi réduit le taux général d'infection, avec ou sans symptômes, de 50%.
"Ces données sur l'utilisation du REGEN-COV comme vaccin passif suggèrent qu'il pourrait à la fois réduire la transmission du virus et réduire la charge virale et le fardeau de la maladie chez ceux qui sont quand même infectés", a dit George Yancopoulos, le président de Regeneron.
Donner des anticorps de synthèse peut aider les personnes présentant le risque de tomber gravement malades en raison d'une immunité faible ou d'antécédents médicaux.
Plusieurs scientifiques ont salué leur potentiel contre le COVID-19, et Eli Lilly ainsi que Regeneron ont reçu des autorisations d'utilisation en urgence pour leurs traitements.
Mais l'adoption d'un tel traitement a été limitée aux États-Unis par plusieurs facteurs, dont le manque d'intérêt de la part des patients ainsi que le manque de personnel et de capacités logistiques des hôpitaux pour les administrer.
Dans son communiqué, Eli Lilly reconnaît certaines de ces difficultés.
"Lilly a eu des retours de la part d'infirmiers et de médecins (...) concernant la complexité et le temps nécessaire pour la préparation et l'administration" du traitement, a affirmé Lilly, précisant travailler avec les autorités sanitaires américaines pour potentiellement réduire le temps d'administration par intraveineuse de 60 à 16 minutes.
AFP/VNA/CVN