>>L'OMS envisage de déclarer une "urgence de santé publique internationale"
>>Les vaccins pour bébés de Pfizer et Moderna sous la loupe des experts américains
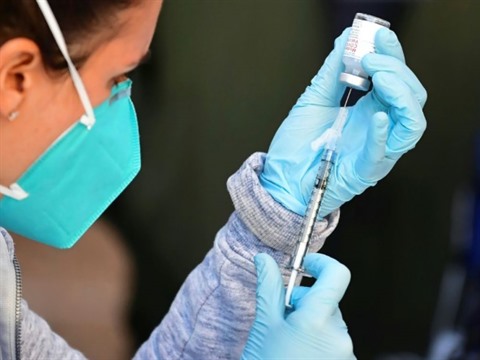 |
| Préparation d'une dose de vaccin contre le COVID-19 à Los Angeles, en février en Californie. |
Pour le vaccin Moderna, la FDA a modifié l'autorisation d'utilisation d'urgence pour inclure son utilisation chez les individus âgés de 6 mois à 17 ans. Le vaccin avait déjà été autorisé pour une utilisation chez les adultes de 18 ans et plus.
Pour le vaccin Pfizer-BioNTech, la FDA a modifié l'autorisation d'utilisation d'urgence pour inclure l'utilisation du vaccin chez les individus âgés de 6 mois à 4 ans. Il avait déjà été autorisé pour une utilisation chez les personnes de 5 ans et plus.
La FDA a souligné que son évaluation et son analyse de l'innocuité, de l'efficacité et des données de fabrication de ces vaccins étaient rigoureuses et complètes, soutenant les autorisations d'utilisation d'urgence.
L'agence est arrivée à la conclusion que les avantages connus et potentiels des vaccins anti-COVID-19 Moderna et Pfizer-BioNTech l'emportent sur les risques connus et potentiels dans les populations pédiatriques autorisées à recevoir chaque vaccin.
La décision de la FDA est intervenue après une réunion de ses conseillers en début de semaine, qui ont voté en faveur de la recommandation des vaccins anti-COVID-19 Moderna et Pfizer-BioNTech pour les enfants dès six mois.